DC诱导分化方法(人和鼠)-简单化
一、什么是DC?
树突状细胞(Dendritic cells,DC)是机体功能最强的抗原呈递细胞(Antigen presenting cells,APC),细胞形态特点是成熟时伸出许多树突样或伪足样突起。DC能高效地摄取、加工处理和呈递抗原,是唯一能够显著刺激初始T细胞(naive T cells)增殖的APC(其他种类的APC如单核巨噬细胞,B细胞等仅能刺激已活化的或者记忆性的T细胞)。因此DC是适应性T细胞免疫应答的唯一始动者。
DC虽然存在于体内多种组织中,但含量很少,无法满足研究或临床治疗的需求。目前,人们尝试多种方法体外诱导培养并扩增DC。对于人,最常用的方法是从人外周血单核细胞(PBMC)诱导DC的产生。而对于小鼠,通常利用骨髓细胞诱导产生DC,即骨髓来源的树突状细胞(Bone Marrow-Derived Dendritic Cells,BMDC)。
二、DC常用诱导方案
因为DC需从其他种类细胞诱导分化而来,且可分为不同的成熟阶段,所以通常分为2个步骤培养:
阶段一:从DC的祖细胞诱导分化为未成熟DC(immature DC,iDC)
① GM-CSF(粒细胞巨噬细胞集落刺激因子)
在DC培养中可促进单核细胞向巨噬细胞样细胞分化,细胞表面MHC II类分子的表达得以提高,从而增强细胞的抗原呈递功能。
② IL-4(白细胞介素-4)
IL-4可在单核细胞诱导成DC的过程中抑制巨噬细胞的过度生长,从而引导单核细胞向DC方向的分化。若不在GM-CSF的基础上添加IL-4,细胞将分化为巨噬细胞。此外,IL-4还能降低细胞表面标志物CD14表达水平。CD14表达降低是单核细胞分化为DC的重要标志。
特点:
该阶段GM-CSF与IL-4共同作用可使单核细胞定向分化为未成熟DC,此时的DC具有较强的抗原摄取与加工能力,但抗原呈递能力较弱。细胞表面中度表达MHC I类、II类分子和B7家族分子(CD80、CD86等),但不表达或低表达CD14。但如果去除两种细胞因子,DC将逆转为巨噬细胞。该阶段的细胞主要功能是抑制T细胞的增殖。
阶段二:从iDC诱导分化为成熟DC(mature DC,mDC)
① TNF-α/IL-1β/IL-6(肿瘤坏死因子-α/白细胞介素-1β/白细胞介素-6)
TNF-α/IL-1β/IL-6三者均为促炎因子,在感染局部和肿瘤部位被诱导产生。三者可上调细胞表面MHC I类、II类分子和B7家族分子(CD80、CD86等)的表达,使未成熟DC分化为成熟DC。
② PGE2(前列腺素E2)
研究表明,在前者三个细胞因子的基础上加入PGE2,可以进一步提高DC的产量、成熟度、迁移能力以及免疫激活能力。因为PGE2可以使DC表面趋化因子受体的表达升高,更容易迁移至淋巴结,引起机体对抗肿瘤的免疫应答。
因此,TNF-α/IL-1β/IL-6/PGE2组合被认为是制备成熟DC的“金标准”,广泛应用于临床。工作浓度分别为:TNF-α(10 ng/mL)、IL-1β(10 ng/mL)、IL-6(1000 U/mL)、PGE2(1 μg/mL)。
③ LPS(脂多糖)
LPS是DC体外完全成熟的强诱导剂。研究表明LPS可以与DC表面的TLR4受体结合,激活下游信号通路,导致DC表面共刺激因子(如CD80、CD86等)与MHC分子表达上调,从而诱导DC成熟,增强其抗原呈递能力。
特点:
该阶段细胞的抗原摄取、加工处理能力减弱,但抗原呈递能力显著增强,可有效激活T细胞,引起免疫反应。诱导成熟后即使去除细胞因子,细胞仍能保持DC的状态和功能。
(一)MoDC的制备流程
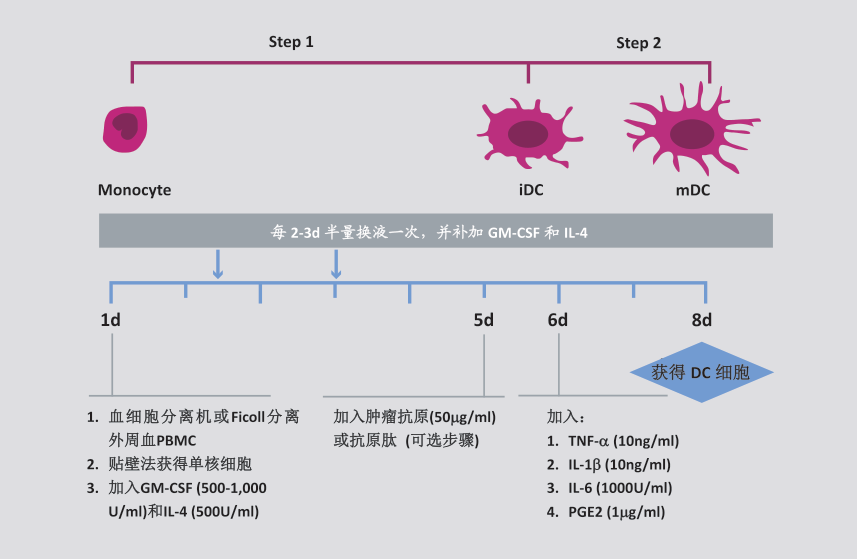
制备步骤
(1) 人外周血单核细胞的获得
利用Ficoll分离液采用密度梯度离心法将收集的外周血进一步纯化出单核细胞(PBMC);
(2) 人MoDC的制备
1. 将步骤1中获得的PBMC用无血清培养液调整细胞浓度至2 × 106/mL,置于培养瓶内;
2. 37℃,5% CO2培养箱中孵育2 h,使单核细胞贴壁;洗去悬浮细胞,在贴壁细胞中加入含重组人GM-CSF(500-1000 U/mL)和重组人IL-4(500 U/mL)的无血清培养液,37℃,5% CO2培养箱中培养,诱导单核细胞向DC分化;
3. 每2-3d半量换液一次,并补足细胞因子;
4. (不做抗原负载,可省略)在培养的第5d,加入肿瘤抗原50 μg/mL,对DC进行抗原负载;
5. 在培养的第6d,加入重组人TNF-α(10 ng/mL)、IL-1β(10 ng/mL)、IL-6(1000 U/mL)、PGE2(1 μg/mL),诱导DC成熟;
6. 培养24h或48h,收获DC,细胞数量应在1 × 106个以上;
7. DC的质检
a. 活细胞比例:台盼蓝染色验证活细胞占比90%以上;
b. 形态学观察:90%以上的细胞半悬浮,细胞有多个树突样突起;
c. 细胞表型分析:常用流式细胞术检测DC表面分子标志CD14、HLA-DR、CD40、CD80、CD83和CD86等,成熟的DC不表达CD14,高表达其他分子。CD83是成熟DC的特异性标志之一,在单核细胞和不成熟DC表面不表达或低表达;
d. 无菌检测:收获细胞前取少量培养物进行细菌、真菌培养,并检测支原体、衣原体,均应为阴性;
e. 内毒素检测:用鲎试剂检测内毒素含量,标准:内毒素含量小于0.5 EU/mL;
(3) 人MoDC的鉴定
1. 准备细胞:取培养的细胞离心(300 g/5 min),弃去上清,加入一定量PBS洗涤一次,弃去上清,弹散细胞,细胞重悬至5 × 106-10 × 106/mL之间;
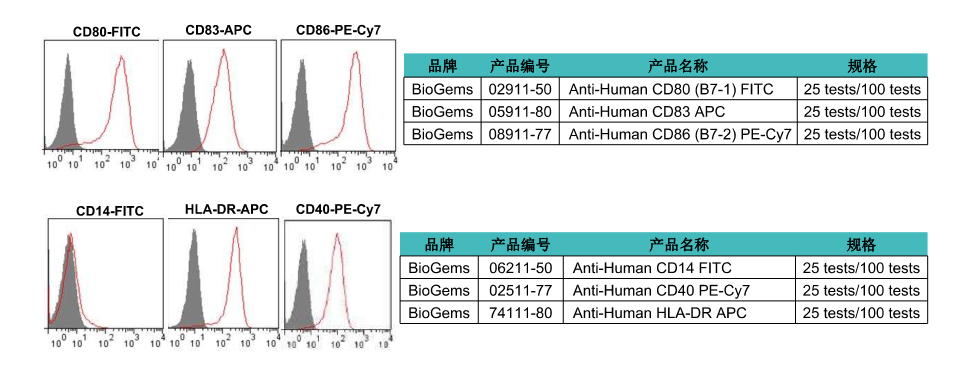
2. 取100 μL的细胞于EP管或流式管中,分两管染色,第一管Anti-human CD80 FITC,Anti-human CD83 APC,Anti-human CD86 PE-Cy7各加5 μL;第二管Anti-human CD14 FITC,Anti-human HLA-DR APC,Anti-human CD40 PE-Cy7各加5 μL;(细胞marker表达量的鉴定应与同型对照比较)
3. 加入相应抗体后混匀,建议轻弹管壁,尽量不用枪头直接吹打,降低对细胞的机械损伤,室温避光孵育15 min,染色过程中再混匀一次;
4. 染色完成后加入1 mL的PBS洗涤细胞,离心300 g/5 min;
5. 弃去上清,弹散细胞,加入500 μL的PBS重悬,上机检测。
Tips:
l DC培养周期较长,诱导分化需要细胞因子,因此细胞比较珍贵,在细胞鉴定过程中能使用最少的细胞得到准确的结果非常有必要,以上染色方案是经过优化,三色组合染色,对仪器要求不高(两激光四通道即可,几乎所有实验室都能达到要求),且不需调节补偿,对结果不影响。
l PeproTech总结了比较齐全的人和小鼠DC诱导分化方案(DC培养手册),从细胞分化,到诱导成熟,再到鉴定,均能提供全方位的解决方案。所需试剂国内均有现货,性价比很高。欢迎联系我们索取DC培养手册。
人DC鉴定结果以及相关抗体
(二)mBMDC的制备流程
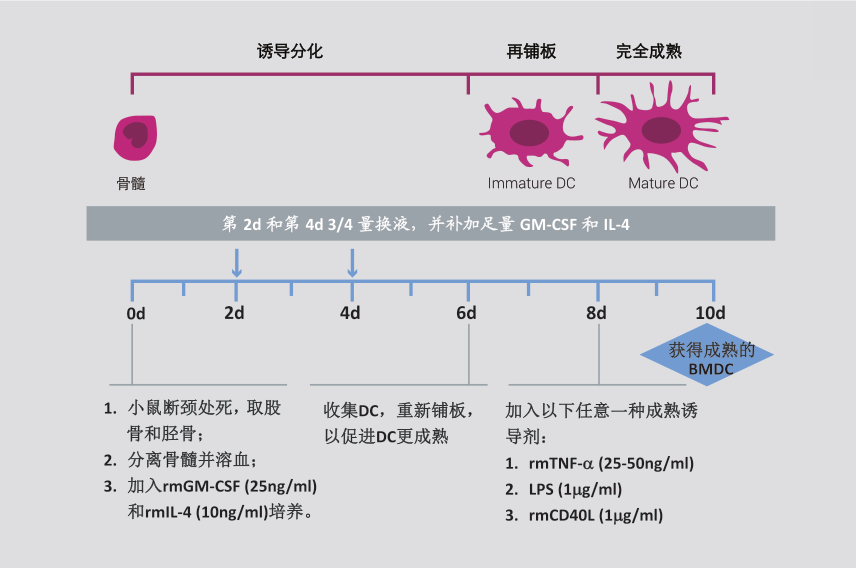
小鼠BMDC大量制备法制备步骤
(1) 小鼠骨髓细胞的获得
1. 将小鼠(6-10周龄)颈椎脱臼法处死,手术解剖取出股骨和胫骨,尽可能去除骨周围的肌肉组织;
2. 将骨头转移至超净台,并用盛有70%酒精的无菌培养皿浸泡2-5 min,以消毒灭菌,然后用无菌的PBS洗2次;
3. 将骨放入另一个盛有PBS的新培养皿中。用剪刀剪去骨两端,再用注射器抽取PBS,针头分别从骨两端插入骨髓腔,反复冲洗骨髓至培养皿中,直至骨完全变白;
4. 收集骨髓悬液,用200目尼龙网滤去小碎片和肌肉组织;
5. 滤过液1200 rpm离心5 min,弃去上清液;
6. 加入2 mL氯化铵红细胞裂解液(1 ×),重悬细胞,室温孵育3-5 min;
7. 加入10 mL PBS中和裂解液的作用,然后1200 rpm离心5 min,弃上清;
8. PBS洗1次,然后用含10%FBS的RPMI 1640培养基重悬细胞,至此已获得小鼠骨髓细胞;
注:因氯化铵细胞裂解液对骨髓细胞有一定的伤害作用,所以尽量缩短溶血时间。
(2) BMDC 的大量制备
1. 步骤(1)中获得的小鼠骨髓细胞计数后用含10% FBS 的RPMI 1640完全培养液调整细胞浓度为2 × 105/mL;
2. 铺至6孔培养板内,每孔5 mL细胞,同时加入重组小鼠GM-CSF(1000 U/mL)和IL-4(1000 U/mL),37℃,5% CO2培养箱培养;
3. 在培养的第4天,向培养体系中补充重组小鼠GM-CSF(1000 U/mL)和IL-4(1000 U/mL);
4. 培养的第7天收集DC,用2-4 mL的RPMI 1640完全培养液重悬,加至等体积的14.5%(w/v)甲泛葡胺上,1200 × g室温离心20 min;
5. 收集中间层,并用RPMI 1640完全培养液洗3次备用。
注:
① 在步骤3中,向培养体系中直接补充细胞因子而不换液的目的是避免出现任何细胞损失,以获得最大量的DC。培养过程中必然会出现培养液变黄的情况,如果不换液而只是添加细胞因子,细胞很快会因为营养耗竭而死亡。所以建议在第4天和第7天时将培养液半量或3/4量吸出,离心后加入含足量GM-CSF和IL-4的新鲜培养液重悬细胞沉淀,然后再将细胞放回至原板。
② 此时的DC为不完全成熟的BMDC,要想进一步成熟,请跳至步骤(3)。
(3) BMDC 的完全成熟
1. 将上述步骤4中收集的BMDC重新铺板,并向培养体系中加入重组小鼠GM-CSF(1000 U/mL)和IL-4(1000 U/mL),以及LPS(1-10 μg/mL);
2. 37℃,5% CO2培养箱继续培养2天,获得成熟的BMDC。
(4) BMDC的鉴定
1. 形态学观察:BMDC多数呈集落生长,细胞有多个树突样突起,成熟的BMDC 更加明显;
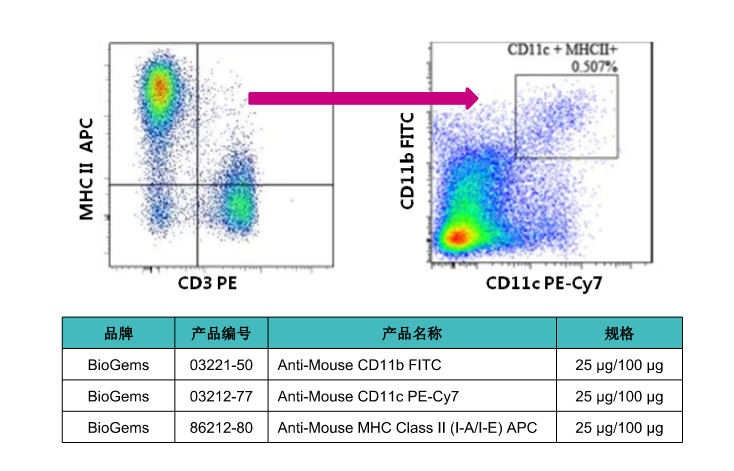
2. 细胞表型分析:流式细胞术检测DC 细胞表面CD11c,CD40,CD80,CD86,MHC Ⅱ 类分子(I-A/I-E)等的表达,BMDC高表达这些分子,完全成熟的BMDC中这些分子的表达会进一步提高。
3. 混合淋巴细胞反应 (MLR):BMDC具有较强的刺激能力,且成熟度越高,刺激能力越强。
小鼠DC鉴定结果以及相关抗体
三、DC诱导相关的细胞因子

四、参考文献
[1] Steinman RM, Cohn ZA. Identification of a novel cell type in peripheral lymphoid organs of mice. I. Morphology, quantitation, tissue distribution. J Exp Med. 1973;137(5):1142-1162.
[2] Bender A, Sapp M, Schuler G, Steinman RM, Bhardwaj N. Improved methods for the generation of dendritic cells from nonproliferating progenitors in human blood. J Immunol Methods. 1996;196(2):121-135.
[3] Romani N, Reider D, Heuer M, et al. Generation of mature dendritic cells from human blood. An improved method with special regard to clinical applicability. J Immunol Methods. 1996;196(2):137-151.
[4] Jonuleit H, Kühn U, Müller G, et al. Pro-inflammatory cytokines and prostaglandins induce maturation of potent immunostimulatory dendritic cells under fetal calf serum-free conditions. Eur J Immunol. 1997;27(12):3135-3142.
[5] Datta J, Terhune JH, Lowenfeld L, et al. Optimizing dendritic cell-based approaches for cancer immunotherapy. Yale J Biol Med. 2014;87(4):491-518.
[6] de Jong EC, Vieira PL, Kalinski P, et al. Microbial compounds selectively induce Th1 cell-promoting or Th2 cell-promoting dendritic cells in vitro with diverse th cell-polarizing signals. J Immunol. 2002;168(4):1704-1709.
[7] 张志伟, 宋鑫. DC-CIK 细胞临床制备规范化研究[J]. 中国肿瘤, 2011, 20(2): 85-88.
[8] Inaba K, Inaba M, Romani N, et al. Generation of large numbers of dendritic cells from mouse bone marrow cultures supplemented with granulocyte/macrophage colony-stimulating factor. J Exp Med. 1992;176(6):1693-1702.
[9] Roney K. Bone Marrow-Derived Dendritic Cells. Methods Mol Biol. 2019;1960:57-62.
[10] Son YI, Egawa S, Tatsumi T, Redlinger RE Jr, Kalinski P, Kanto T. A novel bulk-culture method for generating mature dendritic cells from mouse bone marrow cells. J Immunol Methods. 2002;262(1-2):145-157.
[11] Park HJ, Jang GY, Kim YS, et al. A novel TLR4 binding protein, 40S ribosomal protein S3, has potential utility as an adjuvant in a dendritic cell-based vaccine. J Immunother Cancer. 2019;7(1):60.