类器官研究的最新进展
2025年4月,美国食品药品监督管理局(FDA)宣布:计划逐步取消单克隆抗体及其他药物的动物实验要求。使用“新方法论”(包括 AI 计算模型、人类细胞系、类器官以及器官芯片系统等)替代动物实验,同时使用真实世界数据确定药物的有效性。这标志着以实验动物为研究核心基础的时代正在转变,以AI计算、类器官以及器官芯片系统等为核心的替代方法体系正加速形成。
一、什么是类器官?
类器官,即器官的体外类似物,是模拟人类器官结构和功能的体外模型,其遗传背景、细胞组成和功能更接近人类器官。因此,它避免了动物模型(如小鼠、大鼠)因物种差异导致的药物代谢、毒性反应或疾病机制不匹配的问题。近年来在疾病研究和个性化医疗中展现出巨大潜力。
类器官的核心特征体现为自组装、三维化、功能化——正是这三点,构成了它区别于传统2D细胞培养,并有望补充乃至替代动物模型的技术基础。其生物学特点可概括为细胞多样性、功能模拟、结构仿生。
然而,纯粹的自组装难以复现器官的复杂结构与生理微环境。因此,当前研究形成两条互补路径:一是强化自组装,通过优化基质材料引导细胞自主分化;二是工程化辅助,通过3D打印、微流控等手段施加外部约束,但保留细胞自组织的核心能力。

图1 类器官构建的基本要素(本体、结构、环境、功能)
(一)自组装路径
在类器官培养中,细胞外基质是核心要素。它既提供物理支撑,还可以通过整合素等细胞表面受体与细胞进行双向信号传导,精确调控细胞的黏附、增殖、迁移、分化以及自组织等关键行为。
目前,类器官培养的基底材料主要包括三类:基质胶、脱细胞外基质以及合成材料(如合成水凝胶)。
1. 基质胶
基质胶(Matrigel等)是类器官培养中最常用的ECM替代物。它是从EHS小鼠肉瘤细胞中提取的基底膜蛋白类似物,主要包含层粘连蛋白、IV型胶原蛋白、巢蛋白以及痕量生长因子等。传统基质胶(如Matrigel、BME)虽广泛使用,但存在成分复杂、批次差异、理化性质调控受限以及潜在安全风险等局限。
2. 合成水凝胶
合成水凝胶是通过化学合成方法制备的高分子材料,具有成分明确、批次稳定性高、免疫原性低等优点,其机械性能(如刚度、黏弹性)、降解动力学及生物活性配体均可被精确设计和调控。这有效弥补了基质胶成分复杂、批次差异大、理化性质调控受限等缺陷,使研究者能够单独探究某一微环境因素对类器官发育的影响,为构建标准化、可重复的类器官模型提供了理想平台。
3. 脱细胞外基质
脱细胞外基质(decellularized extracellular matrix, dECM)材料是指使用脱细胞技术从人或其他动物的组织中去除免疫原性细胞成分, 保留ECM成分而形成的生物材料,兼具生物活性与低免疫原性。其突出优势在于组织来源的可选择性——可直接取材于肿瘤等病变组织,重建组织特异性微环境,在肿瘤类器官研究中展现出较基质胶更高的病理相似性。
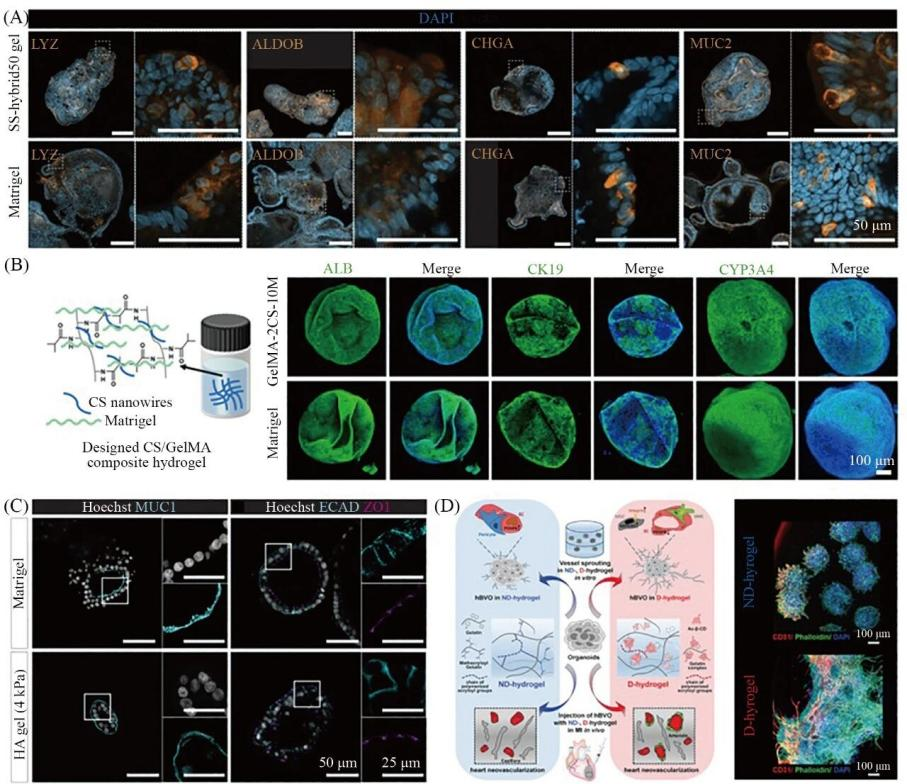
图2 基于化学成分明晰水凝胶的类器官应用[4]
(二)工程化辅助
3D打印:从“自下而上”到“自上而下”
该技术的核心在于结合“自上而下”的打印制造策略(实现对宏观几何结构的精确控制)与“自下而上”的类器官自组织能力(促进细胞间相互作用)。这意味着打印本身是人工干预,打印后的细胞仍可能自组织,但初始空间排布是设计好的。
类器官芯片:引入“外部控制”
芯片通过微流控技术施加流体剪切力、化学梯度、机械刺激等外部控制,这些都不是细胞自发的,而是工程手段模拟的体内生理环境。
二、不同类器官的研究进展
类器官技术已拓展至多个器官系统,各领域的研究重点和应用场景各有侧重。以下首先介绍肠道类器官和胃类器官的最新突破,随后再聚焦于药物筛选核心器官——肝脏,以及功能最为复杂的心脏类器官。
(一)肠道类器官
感染性疾病:2016年ESTES团队利用人肠道类器官实现人诺如病毒稳定体外培养,揭示胆汁酸作为肠道微环境的关键组分,对特定人诺如病毒毒株的感染与复制至关重要;同时,宿主细胞表达的组织血型抗原是病毒感染的先决条件,其表达模式也影响病毒的宿主范围和复制效率。
肿瘤建模:自开创性建立首个源自直肠癌(Colorectal cancer, CRC)患者的活体类器官生物库,结合CRISPR/Cas9技术深入研究,CLEVERS团队证实引入AKPS四重突变(即APC/KRAS/TP53/Smad4)可诱导类器官呈现高度侵袭性表型,此发现提示仅通过四个致癌性突变便足以使正常肠道细胞演变为侵袭性肿瘤细胞;2024年该团队通过选择性压力诱导MLH1缺陷类器官自发癌变,实现动态追踪MSI-H型CRC恶性转化全过程。
重建免疫微环境:2023年WELLS团队在人结肠类器官中重建包含功能性免疫细胞的微环境,在体外重现了从造血内皮细胞到功能性组织驻留巨噬细胞的完整分化过程,实现类器官—免疫共培养。这项技术是研究炎症性疾病以及探索组织驻留免疫细胞发育机制的有效模型,为基础研究提供了强大的新工具。
工程化融合:LUTOLF团队开发“迷你小肠”(mini-guts)及“迷你结肠”(mini-colons)芯片,实现灌流培养与肿瘤发生的光控追踪;2025年建立患者特异性CRC mini-colons,整合肿瘤细胞、肿瘤相关成纤维细胞及肿瘤浸润淋巴细胞,长期模拟复杂的肿瘤微环境,为药物筛选、个体化治疗和肿瘤微环境研究提供了一个强大的新工具。
(二)胃类器官
发育机制:Wnt/β-catenin信号调控胃底型谱系分化,BMP信号调控壁细胞与内分泌细胞生成,AMPK-KLF4-PGC1α通路驱动壁细胞成熟。
感染建模:BARTFELD等利用类器官感染模型验证幽门螺杆菌激活NF-κB通路;MCCRACKEN团队通过显微注射技术模拟早期感染,证实CagA依赖的致病作用及其与β-catenin信号激活、上皮屏障破坏的关联;类器官结合免疫细胞共培养揭示PD-L1、Nod1在感染相关免疫反应中的作用。
个体化治疗:研究人员基于多例胃癌类器官进行了系统性药物筛选实验,在不同患者来源的模型中评估多种化疗药物和靶向药物的体外敏感性。这些药敏结果与患者在临床用药反应高度一致,证实类器官平台在药物反应预测方面具有较高的可靠性。
耐药机制:UKAI团队构建5-FU耐药胃癌类器官模型,揭示KHDRBS3-CD44剪接变体调控机制。这一成果体现了类器官是研究耐药演化过程与关键驱动因子的有力工具,为胃癌乃至其他类型肿瘤耐药提供新思路。
标准化进展:2024年制定《人胃癌类器官构建、质量控制与保藏团体标准》,明确形态学、增殖能力、遗传稳定性及功能特性评价体系。
(三)肝脏类器官在药物筛选中的进展
药物毒性评估:2021年SHINOZAWA等基于238种药物验证肝脏类器官毒性筛选平台,结果表明该平台具有较高的预测准确性,灵敏度88.7%、特异性88.9%;2025年TAN等开发AI模型DILI Tracer,利用肝脏类器官的时空明场图像特征,结合临床DILI等级数据,预测药物性肝损伤风险,总体准确率达82.34%。
代谢与药效研究:NOH团队开发的基于氨基酸代谢分析的无创肝毒性评估体系,利用人诱导多能干细胞衍生的肝脏类器官培养基,鉴定出了天冬氨酸、精氨酸、谷氨酰胺、苯丙氨酸4种氨基酸以及8种氨基酸比值作为标准化肝毒性生物标志物。这为药物肝毒性筛选建立了高可比性的标准化评估体系。LEUNG等开发了一种高通量集成测定法,该技术可实现代谢稳定性与代谢物谱同步测定。
疾病建模:OUCHI等构建了含多种细胞类型的肝脏类器官,通过混合游离脂肪酸,可模拟脂肪性肝炎的渐进性发展过程;研究人员建立α1-抗胰蛋白酶缺乏症、乙肝病毒感染等遗传性与感染性疾病模型;
工程化融合:微流控芯片实现药物浓度梯度生成与细胞培养的集成化,可在单次实验中同时筛选数百至数千个药物样本;3D生物打印模拟肝窦状隙结构;使用旋转生物反应器培养的肝脏类器官,与传统静态培养相比,其白蛋白分泌与药物代谢能力大幅提高。
(四)心脏类器官在心血管发育与疾病研究中的进展
发育模拟:ROSSI团队在类器官分化的第4至第7天,利用单细胞RNA测序识别32种细胞类型。RNA velocity分析进一步揭示了类器官内部关键发育基因的动态表达轨迹。
疾病建模:利用CRISPR/Cas9技术成功构建MYBPC3突变肥厚型心肌病类器官模型;从携带TTN突变的患者获取hiPSCs,构建扩张型心肌病心脏类器官模型;针对KCNH2 p.G628S突变构建长QT综合征类器官模型,该模型IKr钾电流密度下降60%,与临床QTc延长高度吻合。通过冰冻损伤、氧气扩散梯度/去甲肾上腺素刺激模拟心肌梗死病理进程。
血管整合:2025年WU等利用几何微图案化技术构建了包含心肌细胞、心内膜、心外膜细胞、神经细胞在内等多种细胞类型的心脏血管化类器官,模拟早期血管生成。
工程化融合:3D生物打印实现亚毫米级心脏补片(含仿生血管网络);心脏芯片整合微流控与双向流体剪切力,实现高仿真生理/病理环境模拟;2023年PARK团队利用AI辅助自动化分析平台实现搏动频率、收缩幅度等参数实时量化。
转化应用:利用基因编辑(CRISPR/Cas9)校正dystrophin突变,自组装心脏类器官的抗肌萎缩蛋白表达水平恢复85%。纳米线连接类器官移植入缺血再灌注损伤裸鼠心脏,7天和28天存活率约30%,显著改善血管化与心功能。
结语
从FDA的政策转向,到心脏、肠道、肝脏类器官的接连突破,类器官技术正站在从“科研工具”向“临床应用”跨越的关键节点。未来的新药研发,或许将不再是先看小鼠的反应,而是先在培养皿里的“迷你人”身上试一遍。当这些微小的器官在芯片上搏动、代谢,它们带给我们的,将是一个更安全、更高效、更个性化的医学新时代。
免责声明
本文仅供行业学术交流,不构成临床诊疗建议或产品使用指导。类器官技术处于快速发展阶段,具体实验方案需根据研究目的优化调整。本公司提供类器官构建相关试剂,如需订购请联系我们。
参考文献
[1] Ettayebi K, Crawford SE, Murakami K, et al. Replication of human noroviruses in stem cell-derived human enteroids. Science. 2016;353(6306):1387-1393.
[2] van de Wetering M, Francies HE, Francis JM, et al. Prospective derivation of a living organoid biobank of colorectal cancer patients. Cell. 2015;161(4):933-945.
[3] Drost J, van Jaarsveld RH, Ponsioen B, et al. Sequential cancer mutations in cultured human intestinal stem cells. Nature. 2015;521(7550):43-47.
[4] 何雨芯, 张冬卉. 化学成分明晰水凝胶: 推动类器官技术标准化与临床转化的关键三维培养仿生基质[J]. 中国细胞生物学学报, 2025, 47(9): 2153-2162.
[5] Mizutani T, Boretto M, Lim S, et al. Recapitulating the adenoma-carcinoma sequence by selection of four spontaneous oncogenic mutations in mismatch-repair-deficient human colon organoids. Nat Cancer. 2024;5(12):1852-1867.
[6] Múnera JO, Kechele DO, Bouffi C, et al. Development of functional resident macrophages in human pluripotent stem cell-derived colonic organoids and human fetal colon. Cell Stem Cell. 2023;30(11):1434-1451.e9.
[7] Nikolaev M, Mitrofanova O, Broguiere N, et al. Homeostatic mini-intestines through scaffold-guided organoid morphogenesis. Nature. 2020;585(7826):574-578.
[8] Lorenzo-Martín LF, Hübscher T, Bowler AD, et al. Spatiotemporally resolved colorectal oncogenesis in mini-colons ex vivo. Nature. 2024;629(8011):450-457.
[9] Lorenzo-Martín LF, Broguiere N, Langer J, et al. Patient-derived mini-colons enable long-term modeling of tumor-microenvironment complexity. Nat Biotechnol. 2025;43(5):727-736.
[10] McCracken KW, Catá EM, Crawford CM, et al. Modelling human development and disease in pluripotent stem-cell-derived gastric organoids. Nature. 2014;516(7531):400-404.
[11] Panebianco C, Potenza A, Andriulli A, Pazienza V. Exploring the microbiota to better understand gastrointestinal cancers physiology. Clin Chem Lab Med. 2018;56(9):1400-1412.
[12] Bartfeld S, Bayram T, van de Wetering M, et al. In vitro expansion of human gastric epithelial stem cells and their responses to bacterial infection. Gastroenterology. 2015;148(1):126-136.e6.
[13] Holokai L, Chakrabarti J, Broda T, et al. Increased Programmed Death-Ligand 1 is an Early Epithelial Cell Response to Helicobacter pylori Infection. PLoS Pathog. 2019;15(1):e1007468.
[14] Zhao Y, Li S, Zhu L, et al. Personalized drug screening using patient-derived organoid and its clinical relevance in gastric cancer. Cell Rep Med. 2024;5(7):101627.
[15] Ukai S, Honma R, Sakamoto N, et al. Molecular biological analysis of 5-FU-resistant gastric cancer organoids; KHDRBS3 contributes to the attainment of features of cancer stem cell. Oncogene. 2020;39(50):7265-7278.
[16] 苗智峰, 王振宁. 人胃癌类器官构建、质量控制与保藏团体标准[J]. 中华消化外科杂志, 2024, 23(6): 761-769.
[17] Shinozawa T, Kimura M, Cai Y, et al. High-Fidelity Drug-Induced Liver Injury Screen Using Human Pluripotent Stem Cell-Derived Organoids. Gastroenterology. 2021;160(3):831-846.e10.
[18] Tan S, Ding Y, Wang W, et al. Development of an AI model for DILI-level prediction using liver organoid brightfield images. Commun Biol. 2025;8(1):886.
[19] Noh H, Choi S, Park KW, et al. Amino Acid Hepatotoxicity Biomarkers in Human Hepatic Organoids: Promising Standardization of Drug Toxicity Evaluation. ACS Pharmacol Transl Sci. 2025;8(2):510-521.
[20] Leung C, Liu J, Cunico K, Johnson K, Yan Z, Cai J. An Integrated Hepatocyte Stability Assay for Simultaneous Metabolic Stability Assessment and Metabolite Profiling. Drug Metab Dispos. 2024;52(5):377-389.
[21] 李星星, 李亮. 肝脏类器官在药物筛选中的前沿进展: 技术突破与临床转化[J]. 中国细胞生物学学报, 2025, 47(9): 2387-2399.
[22] Pérez-Luz S, Lalchandani J, Matamala N, et al. Quantitative Lipid Profiling Reveals Major Differences between Liver Organoids with Normal Pi*M and Deficient Pi*Z Variants of Alpha-1-antitrypsin. Int J Mol Sci. 2023;24(15):12472.
[23] Ouchi R, Togo S, Kimura M, et al. Modeling Steatohepatitis in Humans with Pluripotent Stem Cell-Derived Organoids. Cell Metab. 2019;30(2):374-384.e6.
[24] Nie YZ, Zheng YW, Miyakawa K, et al. Recapitulation of hepatitis B virus-host interactions in liver organoids from human induced pluripotent stem cells. EBioMedicine. 2018;35:114-123.
[25] Zhai J, Li C, Li H, et al. Cancer drug screening with an on-chip multi-drug dispenser in digital microfluidics. Lab Chip. 2021;21(24):4749-4759.
[26] Bouwmeester MC, Bernal PN, Oosterhoff LA, et al. Bioprinting of Human Liver-Derived Epithelial Organoids for Toxicity Studies. Macromol Biosci. 2021;21(12):e2100327.
[27] Rossi G, Broguiere N, Miyamoto M, et al. Capturing Cardiogenesis in Gastruloids. Cell Stem Cell. 2021;28(2):230-240.e6.
[28] 梁逸云, 孟庆航. 心脏类器官在心血管发育与疾病研究中的应用: 现状与展望[J]. 中国细胞生物学学报, 2025, 47(9): 2332-2348.
[29] Desai D, Song T, Singh RR, et al. MYBPC3 D389V Variant Induces Hypercontractility in Cardiac Organoids. Cells. 2024;13(22):1913.
[30] Hinson JT, Chopra A, Nafissi N, et al. HEART DISEASE. Titin mutations in iPS cells define sarcomere insufficiency as a cause of dilated cardiomyopathy. Science. 2015;349(6251):982-986.
[31] Yuan YC, Wang H, Jiang ZJ, et al. Potassium voltage-gated channel subfamily H member 2 (KCNH2) is a promising target for incretin secretagogue therapies. Signal Transduct Target Ther. 2024;9(1):207.
[32] Voges HK, Mills RJ, Elliott DA, Parton RG, Porrello ER, Hudson JE. Development of a human cardiac organoid injury model reveals innate regenerative potential. Development. 2017;144(6):1118-1127.
[33] Zhang T, Yang S, Ge Y, et al. Unveiling the Heart's Hidden Enemy: Dynamic Insights into Polystyrene Nanoplastic-Induced Cardiotoxicity Based on Cardiac Organoid-on-a-Chip. ACS Nano. 2024;18(45):31569-31585.
[34] Abilez OJ, Yang H, Guan Y, et al. Gastruloids enable modeling of the earliest stages of human cardiac and hepatic vascularization. Science. 2025;388(6751):eadu9375.
[35] Park T, Kim TK, Han YD, Kim KA, Kim H, Kim HS. Development of a deep learning based image processing tool for enhanced organoid analysis. Sci Rep. 2023;13(1):19841.
[36] Varzideh F, Pahlavan S, Ansari H, et al. Human cardiomyocytes undergo enhanced maturation in embryonic stem cell-derived organoid transplants. Biomaterials. 2019;192:537-550.
[37] Erkut E, Yokota T. CRISPR Therapeutics for Duchenne Muscular Dystrophy. Int J Mol Sci. 2022;23(3):1832.
[38] 唐晓芳, 林鑫华. 肠道类器官的发展及其在疾病研究中的应用[J]. 中国细胞生物学学报, 2025, 47(9): 2372-2386.